  |
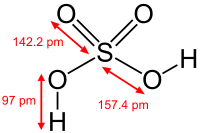
| Struktur Asam Sulfat | sulfuric acid structure |
Ngomong-ngomong masalah asam sulfat, bagaimanakah cara membuatnya?
A. Pembuatan Asam Sulfat
Secara prinsip, pembentukan asam sulfat melibatkan konversi belerang dioksida,SO2, kepada belerah trioksida, yang kemudian dilarutkan ke dalam air guna menghasilkan asam sulfat.
1. Sumber-sumber belerang oksida
Sumber-sumber belerang oksida dapat diperoleh dari unsur belerang, sulfida belerang, gas alam ataupun dari minyak mentah.
belerang oksida dari belerang diperoleh dengan cara menebarkan belerang cair ke dalam suatu dapur yang bersuhu sekitar 1000oC dimana pada suhu setinggi itu belerang akan segera terbakar. Gas dikeluarkan dan dikeringkan dengan cara melewatkan melalui asam sulfat pekat. Sementara belerang oksida yang dihasilkan dari sulfida logam, biasanya merupakan hasil samping pada pengolahan logam itu sendiri, misalnya pada pengolahan zink dari bijih blende.
2. Proses kontak
Pembakaran belerang selalu menghasilkan belerang dioksida dan bukan belerang trioksida, meskipun pembentukan belerang trioksida secara termodinamika lebih disukai daripada pembentukan belerang dioksida (-370 kJ/mol untuk SO3 dan -300kJ/mol untuk SO2) karena tingginya aktivasi untuk oksidasi. Karena itu oksidasi itu memerlukan katalisator yang efektif yang secara komersial dapat diterima. Nah, sekarang kita tahu kan, dalam setiap pengolahan tidak sembarangan reaksi digunakan, karena kita juga memikirkan penghematan dana dan tenaga. Masih ingat cerita pembuatan aluminium? Zaman dahulu aluminium sangatlah mahal, karena proses pengolahannya juga relatif sulit. Pada akhirnya ditemukan cara murah (kalau tidak salah harbes boch, agak lupa saya, nanti saya update untuk membenarkan) untuk pengolahannya, sehingga harganya turun drastis. Cukup deh ceritanya. Nanti dibahas lain kali.
Berikut adalah proses kontak secara garis besarnya:
Pada langkah pertama, kita butuh belerang dioksida sebagai bahan baku, salah satu cara yaitu belerang dipanaskan sehingga didapatkan belerang dioksida:
S (s) + O2 (g) → SO2 (g) delta H (298 K) = -196 kJ/mol
Sulfur dioksida kemudian dioksidasi menggunakan oksigen dengan keberadaan katalis vanadium(V) oksida. Suhu yang diperlukan sekitar 430oC:
2 SO2 + O2(g) → 2 SO3 (g) (dengan keberadaan V2O5)
Reaksi di atas sangat eksotermis, dan oleh sebab itu suhu cepat naik hingga 600oC, dan karena itu campuran as itu didinginkan hingga mencapai suhu semula (430oC) dengan melewatkan pada sebuah penukar panas (pana yang dikeluarkan ini dipakai untuk memanaskan campuran awal). Pada tahap seperti ini, konversi belerang dioksida menjadi belerang trioksida dapat mencapai 66%. Campuran gas ini dilewatkan melalui tiga konventor lagi. Pada tiap tahapan, gas yang mengalir didinginkan menjadi 430oC. dan gas yang keluar dari konventor terakhir, dimana konversi telah mencapai 98%, didinginkan dan diserap diserap ke dalam asam sulfat pekat (98%) untuk menghasilkan asam sulfat 100% atau asam sulfat berasap (oleum)(H2S2O7). Oleum kemudian diencerkan ke dalam air menjadi asam sulfat pekat.
H2SO4 (l) + SO3 → H2S2O7 (l)
H2S2O7 (l) + H2O (l) → 2 H2SO4 (l)
Perhatikan bahwa pelarutan langsung SO3 ke dalam air tidaklah praktis karena reaksi sulfur trioksida dengan air yang bersifat eksotermik. Reaksi ini akan membentuk aerosol korosif yang akan sulit dipisahkan.
SO3(g) + H2O (l) → H2SO4(l)
Sebelum tahun 1900, kebanyakan asam sulfat diproduksi dengan proses bilik.
Untuk mengurangi polusi yang disebabkan oleh SO2 yang tidak mengalami perubahan, di dalam proses yang modern, perencanaan di desain untuk menyerap belerang trioksida dari aliran gas oleh asam sulfat, dilakukan setelah pencampuran gas keluar dari konventor ketiga. Belerang trioksida yang belum teroksidasi bersama udara dimasukkan ke dalam konventor keempat dan kemudian sejumlah belerang trioksida yang terbentuk diserapkan lagi ke dalam asam sulfat. Dalam modifikasi sistem seperti ini, sekitar 0,05% belerang dioksida tetap tidak terkonversi, dan akan lepas ke udara.
Oksidasi katalitik SO2 menjadi SO3 merupakan suatu reaksi eksotermis, karena suatu hasil belerang trioksida yang besar akan lebih disukai pada proses suhu rendah, tetapi juga tidak boleh terlalu rendah, suhu 430oC adalah suhu optimum.
Reaksi konversi di atas terjadi dengan pengurangan volum [ket: dari persamaan 1 diruas kiri ada 3 mol, diruas kanan cuma 1 mol, maka volume kiri: volume kanan=3:1], dan karena itu suatu kenaikan tekanan akan dapat menaikkan konversi pada kesetimbangan, juga kenaikan laju reaksi. Karena baik hasil maupun laju reaksi cukup memuaskan pada tekanan sedikit di atas tekanan udara, maka tidak diperlukan extra belanja guna pembuatan peralatan bertekanan tinggi.
SIFAT-SIFAT ASAM SULFAT;
A SIFAT FISIKA
1. Bentuk-bentuk asam sulfat:
Walaupun asam sulfat yang mendekati 100% dapat dibuat, ia akan melepaskan SO3 pada titik didihnya dan menghasilkan asam 98,3%. Asam sulfat 98% lebih stabil untuk disimpan, dan merupakan bentuk asam sulfat yang paling umum. Asam sulfat 98% umumnya disebut sebagai asam sulfat pekat. Terdapat berbagai jenis konsentrasi asam sulfat yang digunakan untuk berbagai keperluan:
* 10%, asam sulfat encer untuk kegunaan laboratorium,
* 33,53%, asam baterai,
* 62,18%, asam bilik atau asam pupuk,
* 73,61%, asam menara atau asam glover,
* 97%, asam pekat.
Terdapat juga asam sulfat dalam berbagai kemurnian. Mutu teknis H2SO4 tidaklah murni dan seringkali berwarna, namun cocok untuk digunakan untuk membuat pupuk. Mutu murni asam sulfat digunakan untuk membuat obat-obatan dan zat warna.
Apabila SO3(g) dalam konsentrasi tinggi ditambahkan ke dalam asam sulfat, H2S2O7 akan terbentuk. Senyawa ini disebut sebagai asam pirosulfat, asam sulfat berasap, ataupun oleum. Konsentrasi oleum diekspresikan sebagai %SO3 (disebut %oleum) atau %H2SO4 (jumlah asam sulfat yang dihasilkan apabila H2O ditambahkan); konsentrasi yang umum adalah 40% oleum (109% H2SO4) dan 65% oleum (114,6% H2SO4). H2S2O7 murni terdapat dalam bentuk padat dengan titik leleh 36 °C.
Asam sulfat murni berupa cairan bening seperti minyak, dan oleh karenanya pada zaman dahulu ia dinamakan 'minyak vitriol'.
2.Polaritas dan konduktivitas
H2SO4 anhidrat adalah cairan yang sangat polar. Ia memiliki tetapan dielektrik sekitar 100. Konduktivitas listriknya juga tinggi. Hal ini diakibatkan oleh disosiasi yang disebabkan oleh swa-protonasi, disebut sebagai autopirolisis.[3]
2 H2SO4 → H3SO4+ + HSO4−
Konstanta kesetimbangan autopirolisisnya adalah[3]
Kap(25 °C)= [H3SO4+][HSO4−] = 2,7 × 10−4.
Dibandingkan dengan konstanta keseimbangan air, Kw = 10−14, nilai konstanta kesetimbangan autopirolisis asam sulfat 1010 (10 triliun) kali lebih kecil.
Walaupun asam ini memiliki viskositas yang cukup tinggi, konduktivitas efektif ion H3SO4+ dan HSO4− tinggi dikarenakan mekanisme ulang alik proton intra molekul, menjadikan asam sulfat sebagai konduktor yang baik. Ia juga merupakan pelarut yang baik untuk banyak reaksi.
Kesetimbangan kimiawi asam sulfat sebenarnya lebih rumit daripada yang ditunjukkan di atas; 100% H2SO4 mengandung beragam spesi dalam kesetimbangan (ditunjukkan dengan nilai milimol per kg pelarut), yaitu: HSO4− (15,0), H3SO4+ (11,3), H3O+ (8,0), HS2O7− (4,4), H2S2O7 (3,6), H2O (0,1).
B. SIFAT KIMIA
1.Reaksi dengan air
Reaksi hidrasi asam sulfat sangatlah eksotermik. Selalu tambahkan asam ke dalam air daripada air ke dalam asam. Air memiliki massa jenis yang lebih rendah daripada asam sulfat dan cenderung mengapung di atasnya, sehingga apabila air ditambahkan ke dalam asam sulfat pekat, ia akan dapat mendidih dan bereaksi dengan keras. Reaksi yang terjadi adalah pembentukan ion hidronium:
H2SO4 + H2O → H3O+ + HSO4-
HSO4- + H2O → H3O+ + SO42-
Karena hidrasi asam sulfat secara termodinamika difavoritkan, asam sulfat adalah zat pendehidrasi yang sangat baik dan digunakan untuk mengeringkan buah-buahan. Afinitas asam sulfat terhadap air cukuplah kuat sedemikiannya ia akan memisahkan atom hidrogen dan oksigen dari suatu senyawa. Sebagai contoh, mencampurkan pati (C6H12O6)n dengan asam sulfat pekat akan menghasilkan karbon dan air yang terserap dalam asam sulfat (yang akan mengencerkan asam sulfat):
(C6H12O6)n → 6n C + 6n H2O
Efek ini dapat dilihat ketika asam sulfat pekat diteteskan ke permukaan kertas. Selulosa bereaksi dengan asam sulfat dan menghasilkan karbon yang akan terlihat seperti efek pembakaran kertas. Reaksi yang lebih dramatis terjadi apabila asam sulfat ditambahkan ke dalam satu sendok teh gula. Seketika ditambahkan, gula tersebut akan menjadi karbon berpori-pori yang mengembang dan mengeluarkan aroma seperti karamel.
2. Bereaksi dengan Basa
Sebagai asam, asam sulfat bereaksi dengan kebanyakan basa, menghasilkan garam sulfat.
Sebagai contoh, garam tembaga tembaga(II) sulfat dibuat dari reaksi antara tembaga(II) oksida dengan asam sulfat:
CuO + H2SO4 → CuSO4 + H2O
Asam sulfat juga dapat digunakan untuk mengasamkan garam dan menghasilkan asam yang lebih lemah. Reaksi antara natrium asetat dengan asam sulfat akan menghasilkan asam asetat, CH3COOH, dan natrium bisulfat:
H2SO4 + CH3COONa → NaHSO4 + CH3COOH
Hal yang sama juga berlaku apabila mereaksikan asam sulfat dengan kalium nitrat. Reaksi ini akan menghasilkan asam nitrat dan endapat kalium bisulfat. Ketika dikombinasikan dengan asam nitrat, asam sulfat berperilaku sebagai asam sekaligus zat pendehidrasi, membentuk ion nitronium NO2+, yang penting dalam reaksi nitrasi yang melibatkan substitusi aromatik elektrofilik. Reaksi jenis ini sangatlah penting dalam kimia organik.
3. Bereaksi dengan logam
Asam sulfat bereaksi dengan kebanyakan logam via reaksi penggantian tunggal, menghasilkan gas hidrogen dan logam sulfat. H2SO4 encer menyerang besi, aluminium, seng, mangan, magnesium dan nikel. Namun reaksi dengan timah dan tembaga memerlukan asam sulfat yang panas dan pekat. Timbal dan tungsten tidak bereaksi dengan asam sulfat. Reaksi antara asam sulfat dengan logam biasanya akan menghasilkan hidrogen seperti yang ditunjukkan pada persamaan di bawah ini. Namun reaksi dengan timah akan menghasilkan sulfur dioksida daripada hidrogen.
Fe (s) + H2SO4 (aq) → H2 (g) + FeSO4 (aq)
Sn (s) + 2 H2SO4 (aq) → SnSO4 (aq) + 2 H2O (l) + SO2 (g)
Hal ini dikarenakan asam pekat panas umumnya berperan sebagai oksidator, manakala asam encer berperan sebagai asam biasa. Sehingga ketika asam pekat panas bereaksi dengan seng, timah, dan tembaga, ia akan menghasilkan garam, air dan sulfur dioksida, manakahal asam encer yang beraksi dengan logam seperti seng akan menghasilkan garam dan hidrogen.
4. Asam sulfat sebagai agen sulfonasi
asam sulfat pekat dipergunakan dalam kimia organik untuk menggantikan suatu atom hidrogen oleh gugus asam sulfonat.
H2SO4 + CH3C6H5 ---> CH3C6H5SO3 +H2O
Asam sulfat menjalani reaksi substitusi aromatik elektrofilik dengan senyawa-senyawa aromatik, menghasilkan asam sulfonat terkait.

5. Asam sulfat sebagai dehidrator
asam sulfat yang pekat akan menarik unsur-unsur pembentuk air dari sejumlah senyawaan. Sebagai contoh, gula akan dikonversi menjadi karbon dan air. reaksi merupakan reaksi eksotermis yang spektakuler.
6. Asam sulfat sebagai oksidator
Memang asam sulfat bukanlah oksidator sekuat asam nitrat. Sifat oksidatornya baru muncul jika dalam suasan pekat dan panas. Jadi, jika ada soal mengenai reaksi dengan asam sulfat, maka berhati-hatilah. Anda harus melihat kondisinya, kalau encer, maka reaksinya akan seperti reaksi-reaksi asam biasa. Jika pekat, maka reaksinya sudah meningkat menjadi reaksi REDOKS.
Mungkin cukup sekian dulu, capek nulis. Diupdate lain kali.
Sumber: Buku bahan kuliah, dan wikipedia.
sumber buku kuliahnya bisa diperjelas ga ? makasih
ReplyDeleteBuku Anorganik, untuk judul lengkapnya gak tahu gan. Karena bukunya itu fotokopian dari dosen. Halaman depan gak terfotokopi. Tapi kuliahnya anorganik.
Delete